領域代表挨拶
2022年度科研費学術変革領域研究(A)として「生体反応の集積・予知・創出を基盤としたシステム生物合成科学」(領域略称名:予知生合成科学)が採択されました(2022-26年度)。
本研究領域では、天然有機化合物は「探す」もの、という天然物化学分野で半世紀以上続いてきた既成概念から脱却し、天然有機化合物は「創り出す」もの、とする根本的な変革を先導していきます。微生物や植物の進化の歴史が刻み込まれた生物活性天然有機化合物の設計図、すなわち生合成遺伝子は、近年容易に入手可能になりました。これらの膨大な遺伝子資源は実験科学だけでは十分に有効活用することができません。この設計図には、天然有機化合物(完成品)を作り上げるための前駆物質(材料)と生合成反応(作業工程)の情報が、数千から数十万に及ぶ核酸塩基ACGTの組み合わせで暗号化され生合成遺伝子として書き込まれています。この生合成遺伝子を配列情報として捉えて情報処理するアプローチで、天然有機化合物の構造を手早く正確に予測できないでしょうか?また、生合成遺伝子を合理的にデザインすることで、思い描いた化合物を自在に創り出せないでしょうか?2021年夏、AlphaFold2の登場により、配列情報から生合成酵素の立体構造を格段に高い精度で予測できるようになりました。生命情報科学の著しい発展とも相まって、生物合成科学に大きなパラダイムシフトが起きようとしています。多種多様な生合成酵素の機能を的確に予測して、未知の天然有機化合物の構造を予知するとともに、生合成プロセスを自在に改変・拡張し、人工的な物質生産ラインを開拓するアプローチがもうすぐそこまできているように思います。本研究領域では、実験系の天然物化学、生物有機化学、有機合成化学、合成生物学、構造生物学、理論系の計算化学、計算生物物理学、生命情報科学、AIなど、幅広い分野にまたがる多様な研究の融合を通してブレイクスルーを起こし、新たな生物合成科学のパラダイムの確立を目指します。生物合成科学の重要性と将来性を見据えた気鋭の若手研究者が集まって切磋琢磨し、斬新なアプローチを融合した先進的な研究を展開する機会を実現していきたいと考えています。実験科学と理論科学の融合研究にご興味のある方、ぜひご参画ください。

東京⼤学大学院農学生命科学研究科
教授
領域の概要
天然有機化合物は、生体内での作用点やシグナル伝達機構の解明のみならず、創薬への応用の観点からも非常に重要な研究対象です。
フレミングがペニシリンを発見して以来、日本国内からも抗生剤カナマイシン、抗寄生虫薬イベルメクチン、免疫抑制剤FK506に代表される天然有機化合物が発見され、医療に革新をもたらしてきました。これらの天然有機化合物は複雑な構造を持っており、その生合成では、いくつもの生合成酵素が連携し、多段階に及ぶ連続的な反応を精巧に触媒するプロセスで組み立てられます。
近年ゲノム科学の進展により、天然有機化合物の生合成に関連する遺伝情報が大量に入手可能となりました。一方、遺伝子産物である生合成酵素の構造や反応性・選択性に関しては解析や予測が困難であったため、現時点では、地球上に存在する天然有機化合物の生合成経路の多くが未知のままか、手付かずのまま残されています。したがって、これらの未利用資源を有効活用するためには生物合成科学に大きな変革が必要となります。
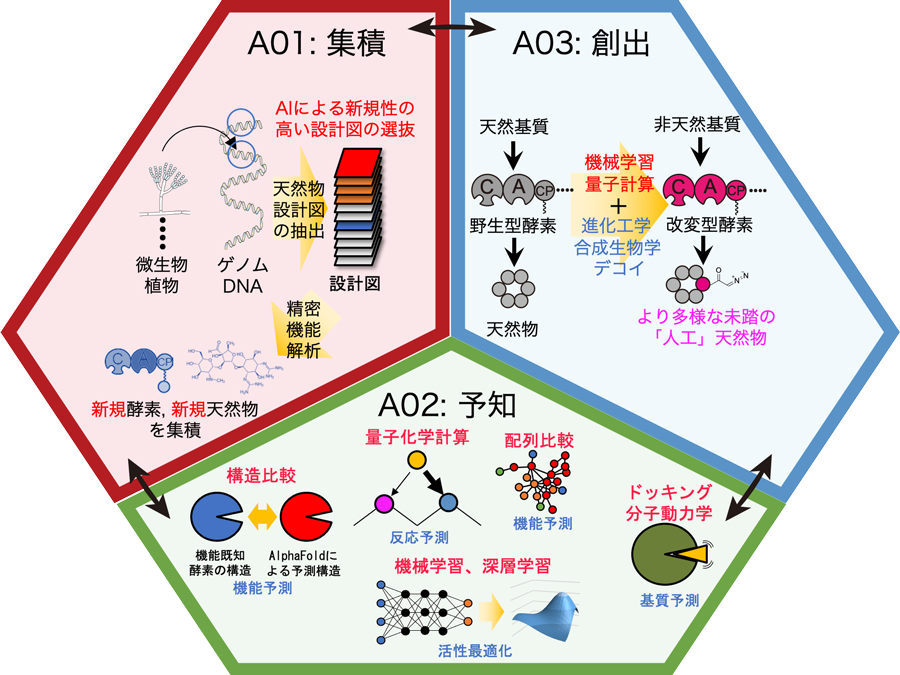
そこで、本研究領域「予知生合成科学」では、天然有機化合物に関連する生体反応の集積(A01)、予知(A02)、創出(A03)の3つの研究項目を柱とし、互いに密接に連携し有機的かつ補完的な共同研究を推進します。本研究領域では、合成生物学と有機合成化学という実験系の2つの学問分野を発展的に融合させるとともに、情報科学や計算科学の理論系と連携したアプローチを追求します。
更に、人工知能(AI)を取り入れて、分子を自在に創り出す革新的な生物合成科学を切り拓きます。なお、本研究領域で開発するAIとして、未活用の天然有機化合物の構造や生合成経路を理論的に予知するシステムの開発を目指しています。この予知システムを構築するためには、帰納的(経験的)な解析手法に加え、分子動力学計算や量子化学計算などの演繹的(理論的)手法が必要不可欠です。既存の方法では解析が困難で未活用資源として眠っているゲノム情報から、この予知システムを駆使して、未知の有益な配列情報を効率的に抽出します。
天然有機化合物の生合成機構を予測・解明するとともに、生物合成と化学合成を融合したプロセスで未踏の天然有機化合物を人工的に生産するアプローチの実現を目指します。